?2023年內蒙古專升本化學基礎考試大綱
摘要:2023年內蒙古專升本招生正式開始,現公布2023年內蒙古專升本化學基礎考試大綱,學生可以通過考試大綱了解相關的考試信息,按照考試大綱進行備考等。具體請見下文。
2023年內蒙古專升本化學基礎考試大綱
普通高等教育專科升本科考試 ( 以下簡稱 “專升本考試”) 是普通高校全日制高職應屆畢業生升入普通高校全日制本科的 選拔性考試,其目的是科學、公平、有效地測試考生在高職階段 相關專業知識、基本理論與方法的掌握水平和分析問題、解決問 題的能力,以利于各普通本科院校擇優選拔,確保招生質量。專 升本考試貫徹黨的教育方針,落實立德樹人根本任務,促進高素 質技術技能人才成長,培養德智體美勞全面發展的社會主義建設者和接班人。
《化學基礎》作為農林生物醫藥類的專業基礎課,該課程考 試旨在選拔具有學習潛能和創新意識的考生。該課程考試說明參 照內蒙古自治區普通高校專升本招考專業對化學基礎的要求和 相關高職高專院校所開設的無機化學、分析化學、有機化學、基 礎化學等課程標準,依據普通高校對新生思想道德和專業素質的 要求,重點考查考生對高職高專階段化學基礎知識、基本技能和 思維方法的掌握程度。
一、考核目標與要求
( 一 ) 知識要求
化學基礎命題對知識內容的要求分為了解、理解 (掌握) 、 綜合應用三個層次,高層次的要求包含低層次的要求。其含義分 別為:
了解:對所學化學知識有初步認識,能夠正確復述、再現、 辨認或直接應用。
理解 (掌握) :領會所學化學知識的含義及其適用條件,能 夠正確判斷、解釋和說明有關化學現象和問題。
綜合應用:在理解所學各部分化學知識之間的本質區別與內 在聯系的基礎上,運用所掌握的知識進行必要的分析、類推或計 算,解釋、論證一些具體、實際的化學問題。
(二) 技能與能力要求
1、接受、吸收、整合化學信息的能力
( 1) 能夠對化學基礎知識融會貫通,有正確復述、再現、辨 認的能力。
(2) 能夠通過對實際事物、實驗現象、實物、模型、 圖形、 圖表的觀察,以及對自然界、社會、生產、生活中化學現象的觀 察,獲取有關的感性知識和印象,并進行初步加工、吸收、有序存儲的能力。
(3) 能夠從試題提供的新信息中,準確地提取實質性內容, 并經與已有知識塊整合,重組為新知識塊的能力。
2、分析問題和解決 (解答) 化學問題的能力
( 1) 能夠將實際問題分解,通過運用相關知識,采用分析、綜合的方法,解決簡單化學問題的能力。
(2) 能夠將分析解決問題的過程和成果,用正確的化學術語 及文字、 圖表、模型、 圖形等表達,并做出解釋的能力。
3 、化學實驗與應用能力
( 1) 了解并初步實踐化學實驗研究的一般過程,掌握化學實 驗的基本方法和技能。
(2) 在解決簡單化學問題的過程中,運用科學的方法,初步 了解化學變化規律,并對化學現象提出科學合理的解釋。
二、考試內容與要求
( 一 ) 無機與分析化學 (分值約 70 分)
對無機與分析化學部分的考查,要求考生系統地掌握物質的 聚集狀態、化學熱力學、化學反應速率、溶液中的四大化學平衡 等化學基本原理;要求考生掌握原子結構、分子結構等基礎知識, 并了解化學變化中物質組成、結構和性質的關系,初步從宏觀和 微觀的角度理解化學變化基本特征;要求掌握定量分析的基本理 論、滴定分析和吸光光度分析的基本方法,樹立量的概念;掌握 基本的化學實驗操作方法。
具體考試范圍和要求如下:
1. 氣體和溶液
( 1) 了解溶液的蒸氣壓、沸點、凝固點、滲透壓和滲透作用 等概念;
(2) 掌握理想氣體狀態方程及其應用;
(3) 掌握道爾頓分壓定律及其應用;
(4) 掌握物質的量濃度、質量摩爾濃度和質量分數等概念;
(5) 理解幾種不同的濃度表示法之間的換算,掌握有關溶液 配制的計算;
(6) 了解難揮發非電解質稀溶液的依數性及其應用。
2. 化學熱力學
( 1) 了解熱力學能、焓、熵和吉布斯自由能等狀態函數的概 念;
(2) 理解熱力學第一定律、第二定律和第三定律的基本內容;
(3) 掌握化學反應的標準摩爾焓變、標準摩爾熵變和標準摩 爾吉布斯自由能變的計算方法;
(4) 會用△G 判斷反應方向;
(5) 了解溫度、壓力和濃度對△G 的影響。
3. 化學平衡和化學反應速率
( 1) 了解化學平衡的特征;
(2) 掌握標準平衡常數和標準吉布斯自由能變之間的關系;
(3) 能寫出不同類型反應的標準平衡常數表達式,并能應用標準平衡常數進行有關化學平衡的計算;能運用多重平衡規則求標準平衡常數;
(4) 了解溫度對標準平衡常數的影響;
(5) 掌握化學平衡移動的定性判據;
(6) 了解化學反應速率的概念及其表示法;
(7) 了解溫度對反應速率影響的阿倫尼烏斯經驗式。
4. 定量分析
( 1) 了解分析化學的任務和作用;
(2) 了解定量分析方法的分類;
(3) 了解定量分析的過程和分析結果的表示方法;
(4) 理解有效數字的意義,掌握它的運算規則;
(5) 了解定量分析誤差的產生及其各種表示方法; 了解提高 分析結果準確度的方法;
(6) 掌握實驗數據處理和結果分析的方法。
5. 酸堿平衡和酸堿滴定法
( 1) 了解近代酸堿理論(重點是酸堿質子理論) 的基本概念;
(2) 掌握一元弱酸、弱堿的解離平衡和多元弱酸分級解離平 衡的計算;
(3) 了解同離子效應和鹽效應對解離平衡的影響;
(4) 了解緩沖溶液原理及緩沖溶液的組成和性質;
(5) 掌握緩沖溶液pH 的計算,并能配制一定pH 的緩沖溶液;
(6) 了解滴定分析中的基本概念——標準溶液、化學計量點、指示劑、滴定終點、滴定誤差; 了解滴定分析過程和方法分類;
(7) 了解滴定分析的標準溶液及基準物,滴定分析的計算;
(8) 了解酸堿指示劑的變色原理、指示劑的變色點、變色范圍;
(9) 掌握強堿 (酸) 滴定一元酸 (堿) 的原理,滴定曲線的概念,影響滴定突躍的因素,化學計量點 pH 值及突躍范圍的計算,指示劑的選擇;
( 10) 掌握酸堿標準溶液的配制及標定;掌握混合堿的分析方 法;
( 11) 了解酸堿滴定法的某些具體應用。
6. 沉淀溶解平衡和沉淀滴定法
( 1) 理解難溶電解質沉淀溶解平衡的特點,會運用溶度積規 則判斷沉淀溶解平衡的移動及有關計算;
(2) 掌握沉淀滴定法的基本原理;
(3) 了解沉淀滴定法的實際應用。
7. 氧化還原反應和氧化還原滴定法
( 1) 掌握氧化還原反應的基本概念及離子電子法配平氧化還 原反應方程式;
(2) 了解原電池的組成, 電極反應, 電池符號; 了解電極電 勢的概念;
(3) 了解能斯特方程,能正確書寫能斯特方程;
(4) 掌握原電池電動勢與電池反應的關系,標準電動勢與氧化還原反應標準平衡常數 K 的關系;
(5) 掌握應用標準電極電勢判斷氧化劑和還原劑的強弱,能 用電極電勢判斷氧化還原反應的方向和完成程度;掌握運用元素電位圖判斷處于中間價態物質能否發生歧化;
(6) 了解氧化還原滴定的基本原理; 了解條件電極電勢的概念,條件平衡常數的概念,氧化還原滴定對條件電極電勢差值的要求;
(7) 了解氧化還原反應方向、進行的程度、氧化還原滴定曲 線及指示劑的選擇;
(8) 了解常用的氧化還原滴定法—— 高錳酸鉀法、碘量法和 重鉻酸鉀法。
8. 原子結構和分子結構
( 1) 了解核外電子運動的特性—— 波粒二象性、量子化、不 確定原理、波函數與原子軌道,原子軌道和電子云角度分布圖和徑向分布圖;
(2) 了解四個量子數的物理意義,相互關系及合理組合;
(3) 掌握核外電子排布的原理,能熟練寫出一般元素原子核 外電子排布式;
(4) 了解離子鍵的本質和離子鍵特征;
(5) 了解價鍵 ( 電子配對) 理論,共價鍵的特性;
(6) 理解σ鍵和π鍵,雜化軌道理論的要點,雜化軌道的類型 和簡單分子的空間構型關系;
(7) 了解分子間力 ( 范德華力、氫鍵) 及其對物質物理性質 (熔沸點、溶解度等) 的影響。
9. 配位化合物和配位滴定法
( 1) 了解配合物、螯合物的概念以及配合物的組成;
(2) 掌握配合物的命名;
(3) 了解配合物價鍵理論的要點, 了解配位鍵的形成條件;
(4) 了解酸效應系數以及控制溶液 pH 值的重要意義,用條 件穩定常數來判斷配位滴定的可能性、影響EDTA 與金屬離子配合物的穩定性因素;
(5) 掌握如何選擇合適的滴定條件以使配位反應進行更完 全;
(6) 了解常用的配位滴定指示劑的變色范圍; 了解配位滴定 的方式和某些具體應用。
10. 分光光度法
( 1) 了解光度分析法的基本概念及其特點;
(2) 掌握吸光光度法的原理,吸收光譜和溶液的顏色關系, 朗伯- 比耳定律及其偏離的原因;
(3) 了解顯色反應及影響因素,測量方法及儀器;
(4) 了解分光光度法儀器測量誤差及其消除。
11. 化學實驗基礎 (包括無機、分析和有機實驗)
( 1) 了解常見的化學實驗儀器、實驗裝置;
(2) 掌握化學實驗基本操作:儀器洗滌和干燥、 電子天平稱量、溶液的配制、滴定分析、蒸發、萃取、過濾、重結晶以及蒸餾等;
(3) 掌握滴定分析和可見分光光度法的原理和方法。
(二) 有機化學 (分值約 30 分)
對有機化學部分的考查,要求考生系統地掌握有機化學的基本概念、基本理論、基本技能。掌握各類常見有機化合物的命名、 主要性質、制備方法、結構與性質的關系及相互轉化的方法;掌 握不同有機化合物結構的常用鑒定方法,能夠設計常見有機化合 物的鑒別方案;能夠依據有機化學反應原理,完成有機化學反應 方程式,結合實驗現象推測有機化合物結構,設計有機化合物合 成路線。具體考試范圍和要求如下:
1. 有機化合物的組成與結構
( 1) 了解有機化合物和有機化學概念;掌握同分異構體、官 能團、同系物等基本概念;
(2) 了解常見有機化合物的結構和成鍵特點,理解有機化合 物分子中的電子效應 (誘導效應、共軛效應) 及其對化合物性質
的影響, 了解雜化軌道等化學理論;
(3) 了解確定有機化合物結構的化學方法和物理方法;
(4) 掌握有機化合物的分類方法 (碳骨架分類和官能團分 類 ) ,掌握主要官能團
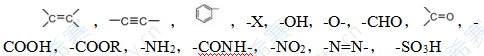 等對應的代表性化合物;
等對應的代表性化合物;
(5) 掌握有機化合物的系統命名法,官能團的最低系列原則 和取代基的次序規則,掌握分子構型的標記方法;了解有機化合物的普通命名法、衍生物命名法、常用俗名等;
(6) 能夠正確書寫有機化合物的同分異構體。
2. 烷烴
( 1) 了解烷烴、環烷烴的通式和構造異構;
(2) 掌握烷烴、環烷烴的分類和命名;
(3) 理解烷烴、環烷烴的物理性質和同系物規律;
(4) 掌握烷烴的化學性質:氧化、取代反應;
(5) 掌握環烷烴的化學性質:氫解、 鹵解、酸解—小環不穩 定性;
(6) 了解烷烴的來源, 甲烷等烷烴的重要代表物的性質和用 途。
3. 不飽和烴
( 1) 掌握單烯烴、共軛二烯烴、炔烴及其結構;
(2) 掌握單烯烴系統命名規則,炔烴系統命名規則;
(3) 掌握不飽和烴的氧化反應、加成反應、聚合反應;端基炔的特性;順反異構現象及其產生的原因;共軛效應;共軛二烯烴的加成反應;
(4) 理解原子或基團的電子效應;
(5) 了解乙烯、 乙炔、1,3- 丁二烯、異戊二烯等重要代表物 的性質和用途。
4. 芳香烴
( 1) 理解芳香烴的分類和命名;
(2) 掌握單環芳香烴和稠環芳香烴的結構和取代 (硝化、 鹵化、磺化、烷基化、酰基化 ) 、加成 (加氫、加氯 ) 、氧化 (側 鏈α-H 的氧化) 等性質;
(3) 理解苯環上取代基的定位規律;
(4) 掌握鑒別常見的環烷烴、苯及其同系物和其它烴;
(5) 了解苯及其同系物、萘、蒽、菲等芳香烴的重要代表物 的性質和用途。
5. 鹵代烴
( 1) 了解鹵代烴的結構、分類,掌握命名;
(2) 了解鹵代烴的制法;
(3) 了解鹵代烴的物理性質;
(4) 掌握鹵代烴的化學性質:①鹵原子的親核取代:水解、 醇解、氰解、氨解與硝酸銀- 乙醇溶液的反應,與碘化鈉-丙酮溶液反應,與金屬鎂反應—格氏試劑的生成;②消除反應;
(5) 了解三氯甲烷、氯乙烯、 四氟乙烯等鹵代烴重要代表物 的性質和用途。
6. 醇、酚、醚
( 1) 了解醇、酚、醚的結構、分類和命名;
(2) 了解醇、醚的制法;
(3) 了解醇、酚、醚的物理性質;
(4) 掌握醇的化學性質:羥基上氫的反應,羥基的親核取代 反應、羥基的消除反應 (脫水) 、醇的氧化或脫氫反應;
(5) 掌握酚的弱酸性;酚與三氯化鐵的顯色反應;酚苯環上 氫原子的取代反應;酚的氧化反應;
(6) 掌握醚的化學性質:①未共用電子對的反應— 烊鹽生成、 配位化合物生成;②醚鍵的斷裂 (與 HI 、△ ) ;③α-H 的過氧化反應;
(7) 掌握鑒別常見的醇、酚和醚。
7. 醛、酮
( 1) 了解醛、酮的分子結構、分類和命名;
(2) 了解醛、酮的物理性質;
(3) 掌握醛和酮的化學性質:羰基的親核加成:加氫氰酸, 加亞硫酸氫鈉,加格氏試劑,加醇與氨的衍生物的縮合 (加成+ 消除) ,與碳負離子即與具有α-H 的醛 ( 酮 ) 的縮合;氧化還原; α-H 的活潑性; 鹵化和碘仿反應等;
(4) 了解重要的醛、酮的性質及其用途。
8. 羧酸及其衍生物
( 1) 了解羧酸及其衍生物的結構、分類與命名;
(2) 了解羧酸及其衍生物的物理性質;
(3) 掌握羧酸的化學性質:羧羥基的親核取代—衍生物的生成,羧羰基的還原,α-H 的鹵化—取代酸的生成,酸性,二元羧酸脫羧、脫水,鈍化苯環的間位親電取代;
(4) 掌握羧酸衍生物的化學性質:酯、酰胺的水解和酯的醇解,酯的還原和克萊森酯縮合,酰胺的霍夫曼降解反應;
(5) 了解重要的羧酸及其衍生物的性質和用途。
9. 含氮有機化合物
( 1) 了解硝基化合物的分子結構命名規則; 了解胺的分類、 命名規則和結構;
(2) 掌握硝基化合物化學性質:芳環上硝基的還原反應、硝 基對芳環親電取代反應的致鈍作用;
(3) 了解胺的物理性質;
(4) 掌握胺的化學性質:①堿性;②氮上的烴基化;③氮上 的酰基化,與對甲苯磺酰氯的反應;④與亞硝酸反應生成重氮鹽;
⑤氨基對苯環上的親電取代反應的致活作用;⑥胺的氧化;
(5) 了解季銨結構、季銨鹽、季銨堿及其堿性;
(6) 理解芳香族重氮鹽和偶氮化合物的生成、性質及其在有 機合成中的應用。
三、考試形式與參考題型
( 一 ) 考試形式
考試采用閉卷、筆試形式。考試時間為 150 分鐘,全卷滿分 100 分。考生可以攜帶無聲無文本編輯功能、不帶存儲功能的計 算器進入考場。
(二) 參考題型
考試題型包括單項選擇題、填空題、判斷題、應用題等,也 可以采用其它符合學科性質和考試要求的題型。
四、參考書目
含有上述考試內容的《無機及分析化學》《有機化學》《基 礎化學》等參考書目。
延伸閱讀
- 2023年內蒙古專升本考試大綱匯總
- 2023年內蒙古專升本藝術基礎考試大綱
- 2023年內蒙古專升本醫學基礎考試大綱
- 2023年內蒙古專升本經濟學與管理學基礎考試大綱
- 2023年內蒙古專升本化學基礎考試大綱
- 2023年內蒙古專升本高等數學Ⅱ考試大綱

專升本微信公眾號

掃碼添加
專升本備考資料免費領取
去領取












 掃描二維碼
掃描二維碼